O que é a Conitec? – Por dentro do processo
Comunicação IUPV - 07/08/2020 07:26
No dia 09 de julho de 2020, a Comissão Nacional de Incorporação de Tecnologias no Sistema Único de Saúde (Conitec), em sua 88º Reunião, realizou a apreciação inicial dos medicamentos Kalydeco (ivacaftor) e Orkambi (lumacaftor/ivacaftor). Infelizmente, a recomendação preliminar da Comissão foi desfavorável à incorporação dos dois medicamentos com encaminhamento para consulta pública.
É muito provável que, antes dessa reunião acontecer, você nunca tenha ouvido falar na Conitec ou, caso já tenha ouvido, tenha dúvidas sobre o que é a Comissão. Por isso, a coluna Por dentro do processo, criada pela equipe do Unidos pela Vida – Instituto Brasileiro de Atenção à Fibrose Cística, traz agora informações que vão lhe ajudar a responder a pergunta: o que é a Conitec? Além disto, o Unidos pela Vida já disponibilizou vários outros materiais que também abordam este tema, e que estão listados ao final deste texto.
Entendendo a Conitec
Criada em 28 de abril de 2011 pela lei nº 12.401, a Comissão Nacional de Incorporação de Tecnologias no Sistema Único de Saúde (Conitec) tem como objetivo assessorar o Ministério da Saúde nas atribuições relacionadas à incorporação, exclusão ou alteração de tecnologias em saúde no SUS. Além disso, a Comissão também trabalha na constituição ou alteração de Protocolos Clínicos e Diretrizes Terapêuticas (PCDT).
Por meio desse trabalho, a Conitec busca dar mais agilidade, transparência e eficiência durante a análise dos processos de incorporação de tecnologias em nosso país, e é assistida pelo Departamento de Gestão e Incorporação de Tecnologias e Inovação em Saúde (DGITIS).
Como é formada?
O funcionamento da Conitec é regulamentado pelo decreto nº 7.646 de 21 de dezembro de 2011, e a estrutura da Comissão é formada pelo Plenário e pela Secretaria-Executiva.
Plenário: formado por representantes de cada Secretaria do Ministério da Saúde, do Conselho Federal de Medicina, do Conselho Nacional de Saúde, do Conselho Nacional das Secretarias Estaduais de Saúde, do Conselho Nacional de Secretarias Municipais de Saúde, da Agência Nacional de Saúde Suplementar e da ANVISA.
Secretaria-Executiva: formada pelo Departamento de Gestão e Incorporação de Tecnologias e Inovação em Saúde (DGITIS).
Qual o papel de cada fórum?
Agora que você já sabe por quem é composta a Conitec, vamos explicar a atuação dos dois fóruns citados acima. Começamos com o Plenário, que é responsável por fazer a emissão de recomendações sobre a incorporação, exclusão ou alterações de tecnologias no SUS, além de ser responsável por constituir ou alterar PCDT e atuar na atualização da Relação Nacional de Medicamentos Essenciais (RENAME).
Já a Secretaria-Executiva é responsável pela gestão e coordenação das atividades da Conitec, além de atuar na emissão de relatórios técnicos sobre a tecnologia avaliada, levando em consideração as evidências científicas, a avaliação econômica e o impacto da incorporação da tecnologia no SUS.
Incorporação de novas tecnologias
O fluxo de incorporação de novas tecnologias tem início justamente quando a Conitec recebe o pedido de incorporação e faz toda a análise documental e dos estudos apresentados pelo demandante. É possível que a Comissão solicite estudos e pesquisas complementares, caso necessário, em algumas avaliações.
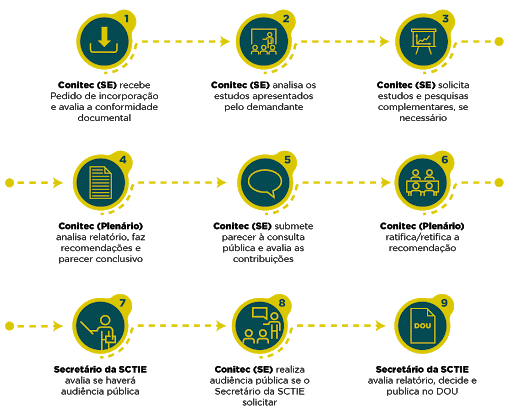
O processo segue com a apreciação inicial do Plenário da Conitec em relação a tecnologia, onde a Comissão faz a análise do relatório e sua recomendação inicial. No caso dos medicamentos Kalydeco e Orkambi, essa etapa do processo aconteceu justamente no dia 09 de julho de 2020, durante a 88º Reunião da Conitec. Na sequência, é aberta a consulta pública, que fica disponível por 20 dias. Após esse período, a Conitec avalia todas as contribuições recebidas e ratifica ou retifica a recomendação preliminar feita durante a plenária.
Por fim, essa recomendação final da Conitec é enviada, por meio de um relatório técnico, ao Secretário de Ciência, Tecnologia, Inovação e Insumos Estratégicos do Ministério da Saúde (SCTIE/MS), responsável pela decisão final sobre a incorporação da tecnologia no SUS.
Importante: para que um medicamento ou tecnologia seja avaliado para incorporação no SUS, primeiro ele precisa ser aprovado pela Agência Nacional de Vigilância Sanitária (ANVISA).
Segue com dúvidas?
Sabemos que, no início, tudo pode parecer muito difícil ou até mesmo burocrático para o entendimento, por isso, caso siga com dúvidas, você pode entrar em contato com o Unidos pela Vida pelo telefone (41) 99636-9493 ou e-mail [email protected]. Conhecer todos os processos que envolvem a incorporação de um medicamento ou tecnologia no SUS é um passo fundamental para termos mais conhecimento sobre nossos direitos, por isso, não hesite em entrar em contato conosco. Vamos lhe ajudar da melhor maneira possível!
Outros conteúdos sobre a temática:
O que é a plenária da Conitec? – Por dentro do processo
Consulta Pública – Por dentro do processo
Consulta Pública da Conitec é tema da quarta edição do Bate-papo sobre Fibrose Cística
Por Kamila Vintureli
Referências:
http://conitec.gov.br/entenda-a-conitec-2
http://www.planalto.gov.br/ccivil_03/_Ato2011-2014/2011/Lei/L12401.htm
Nota importante: As informações aqui contidas tem cunho estritamente educacional. Em hipótese alguma pretendem substituir a consulta médica, a realização de exames e ou, o tratamento médico. Em caso de dúvidas fale com seu médico, ele poderá esclarecer todas as suas perguntas.


